EIおよびCI(PCI/NCI)の3つのモードを単一イオン源で測定可能な
革新的なMulti-Mode Source™(MMS™)<ホワイトペーパー>
概要
Multi-Mode Source™ (以下MMS)は、⾼分解能GC-TOFMSにおいて汎⽤的に利⽤される電⼦イオン化(以下EI)法による測定と化学イオン化 (以下CI)法による測定を容易に切り替えて取得できるイオンソースとして新たに開発されました。ソフトウェア操作のみでEIとCIの設定を切り替えることが可能なため、イオン源の交換や調整に費やす時間は必要ありません。そのため急遽、分⼦量の確認にCI測定が必要な場合においても、すぐにイオン化モードを切り替えて測定することができます。MMSは、主に定性分析で⾼分解能GC-TOFMSを利⽤しているユーザーに最適なイオン源になります。
1.緒⾔
EI法はGCMS分析において汎⽤的に利⽤されるイオン化法です。NISTやWileyといった市販のマススペクトルライブラリが充実していることから、EI法は定性分析に幅広く利⽤されています。しかしながら、マススペクトルライブラリに⽬的の化合物が登録されていない場合、解析作業は困難を極めます。
マススペクトルの解析を⾏うためには、⾼分解能GC-TOFMSが有⽤ですが、EI法は⾼エネルギーの熱電⼦を衝突させてフラグメンテーションを起こす特性を利⽤していることから、化合物の構造によっては分⼦イオンが検出されません。
代表的なソフトイオン化法である正化学イオン化(以下PCI)法は、メタンやイソブタンといった試薬ガスをイオン源内でイオン化させ、⽣成した反応イオンが⽬的化合物と分⼦-イオン間反応を起こさせます。間接的なイオン化反応のため、EI法と⽐較してフラグメンテーションを起こしにくく、分⼦量情報の取得に適しています。特にEI測定においてマススペクトルライブラリで同定できない場合、分⼦量情報はマススペクトル解析において⾮常に重要になります。通常EI法とCI法のイオン源は、下図(Fig.1)のようにそれぞれ専⽤のイオン源を⽤いています。
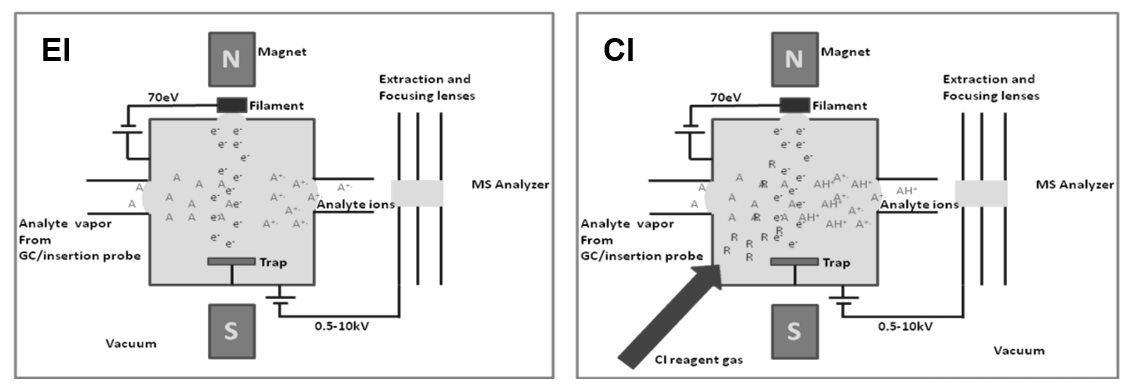
Fig.1 各イオン化用のイオン源の模式図
EIイオン源は、フィラメントから発⽣した熱電⼦をなるべく多く取り込むために、熱電⼦⼊射⼝の⽳が⼤きく設計されています。また、イオン出射⼝も迅速かつ効率よくイオンをフライトチューブに送り込ませるため⽳径が⼤きくなります。CI⽤イオン源はイオン化した試薬ガスとの分⼦-イオン間反応であることから、イオン源内に試薬ガスを充満させる必要があるため、熱電⼦⼊射⼝およびイオン出射⼝の⽳は⾮常に⼩さく設計されています。さらに負化学イオン (以下NCI)源は PCIイオン源よりも熱電⼦⼊射⼝およびイオン出射⼝の⽳径は⼤きくなっており、NCIイオン源で EIや PCI測定を⾏う簡易的な EIおよびCIモードを利⽤することができます。しかし、NCIでの簡易 EIモードでは、フィラメントからの熱電⼦をイオン源内に多く取り込むことが難しいため、微量濃度の分析には向いていません。そのため微量分析において、EIおよび PCI分析を⾏う場合には、従来通りイオン源を交換する必要があり、交換から焼き出し、パージに⻑い時間がかかることが問題となっていました。
2.Multi-Mode Source(MMS)の特徴
イオン源の切り替えによる作業を軽減するため、Pegasus HRT+およびPegasus HRT+4Dに対応する新しいイオン源が開発されました。MMSは、下図 (Fig.2)に⺬す通り、イオン化室が2つ存在しておりソフトウェア上でモードを簡単に切り替えることができ、連続分析のシーケンス内で異なるイオン化モードを設定することも可能です。⼀般的にEIイオン源 からCIイオン源への切り替え作業⾃体は1時間程度で完了しますが、PCIモードではその後、2時間程度システムの焼き出しおよびパージを⾏う必要があります。またNCIを稼働させる場合には、最適な感度を得るために⼀晩焼き出しすることが推奨されています。MMSは、これまでCI法の利⽤に消極的であったユーザーに、PCIおよびNCI利⽤の選択肢を広げます。
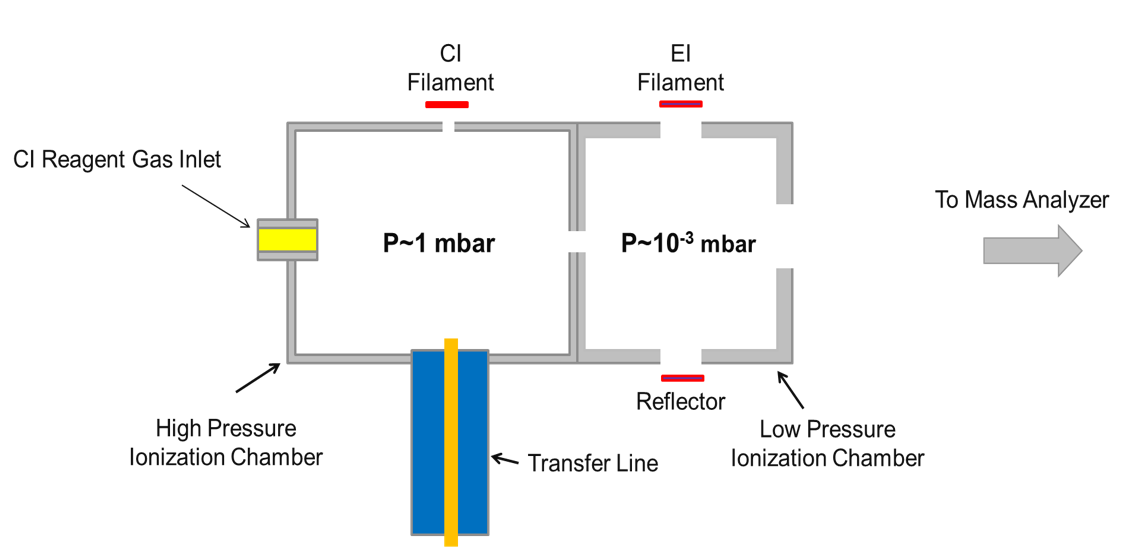
Fig.2 Multi-Mode Source™ (MMS)の概略図
2‐1.MMSにおけるEI測定とマススペクトル
下図(Fig.3)は、MMSのEIモードで取得されたマススペクトルになります。この例では、分⼦イオンといくつかのフラグメントイオンの⽣成が確認できます。
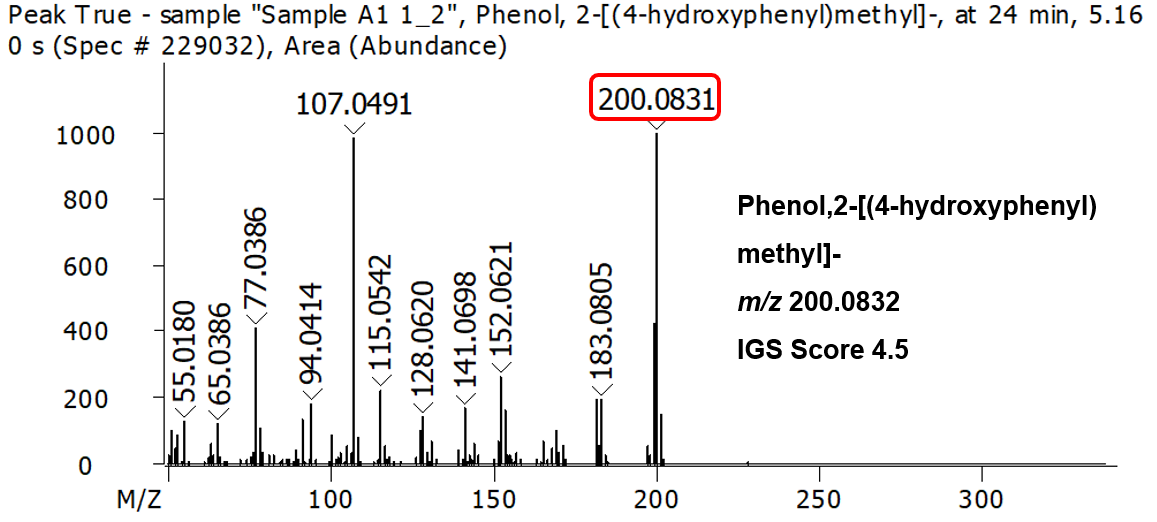
Fig.3 Pegasus HRT EIモードによるマススペクトル例
EI法は、フラグメンテーションの再現性が⾮常に⾼いため、未知のスペクトルをスペクトルライブラリと照合し、その⼀致率から該当する化合物情報を取得することがGCMS分析において最も⼀般的な定性⽅法となります。
⾼分解能型質量分析装置を使⽤する場合は、その正確な質量情報を使⽤して、分⼦イオンとフラグメントイオンの解析にさらに役⽴てることができます。 Pegasus HRT+シリーズでは、1 ppm以内の安定した質量精度と正確な同位体存在⽐、RDBE値および各フィルターによる総合的な評価から、分⼦イオン、フラグメントイオンさらにニュートラルロスの組成式を絞り込むことが可能です。Fig.3のマススペクトル中の分⼦イオンの実測値は200.0831、理論値は200.0832であり、質量誤差はわずか-0.41 ppmでした。さらに専⽤ソフトウェアであるChromaTOF®のIGS™ 機能Identification Grading Syste™)では、従来のライブラリとの⼀致率に加えて分⼦イオン、フラグメントイオンについて精密質量実測値とライブラリヒットの元素組成による精密質量理論値とを確認し、それらの⼀致率から独⾃のIGSスコアを算出します。IGSスコアが⾼いほど、同定の信頼性は⾼くなります。Fig.3のマススペクトルは、IGSスコア4.5/5.0、ライブラリ⼀致率935/1000とどちらも⾼い値を⺬したPhenol,2-[(4-hydroxyphenyl)methyl]-と同定されました。
さらに、リテンションインデックス値による絞り込みも可能であり、より確信度の⾼い定性分析をサポートすることがきます。
2‐2.MMSにおけるPCI測定とマススペクトルと感度
前述したEI法による測定は、GCMS分析において最も⼀般的な測定法ではありますが、⾼エネルギーの熱電⼦を衝突させてフラグメンテーションを起こす特性を利⽤していることから、飽和炭化⽔素化合物など化合物の構造によっては分⼦イオンが検出されない場合があります。そのような化合物の分⼦イオンの検出には、分⼦量情報の取得に適したイオン化法であるCI法が有効です。
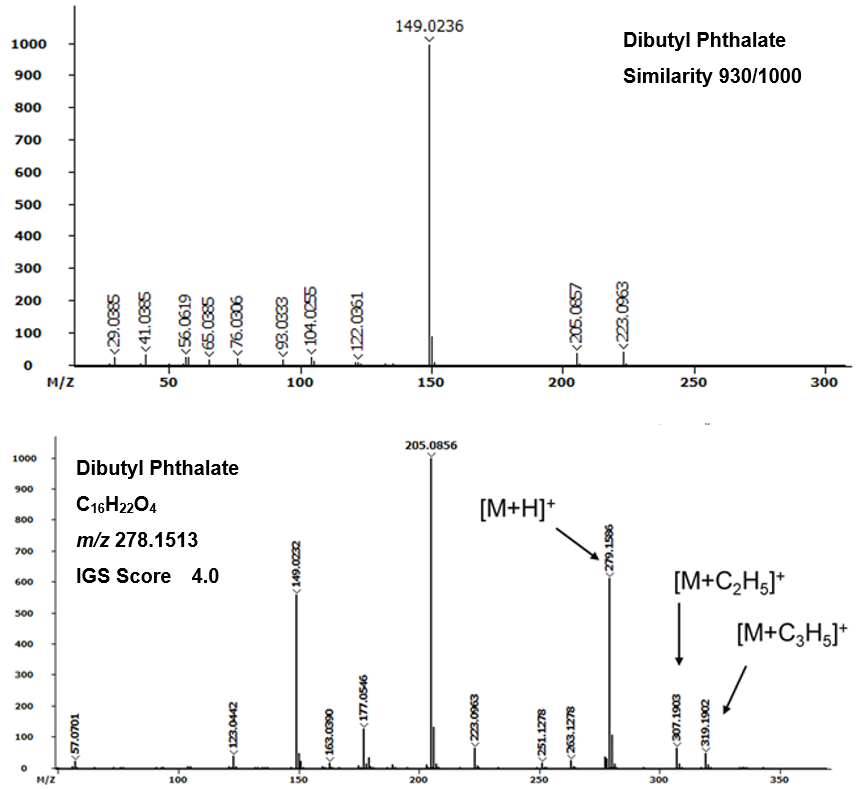
Fig.4 Pegasus HRT EI(上図)およびPCI(下図)モードによるマススペクトル
上図は、同試料をEIおよびPCIモードにより測定を⾏ったマススペクトルになります。EIモードでは、ライブラリ検索でDibutyl Phthalateが⾼い⼀致率でヒットしましたが、分⼦イオンは確認できませんでした。⼀⽅、反応ガスにメタンを⽤いた + + CI分析結果からは、プロトン付加イオン[M+H]+をはじめ、 [M+C2H5]+ および+[M+C3H5]+が検出され、分⼦イオンピークの精密質量から組成式C16H22O4が質量誤差1.02ppmで算出されました。尚、前述したとおり、正確な組成式を決定するには、⾼い質量精度と⾼分解能だけでは不⼗分であり、同位体存在⽐の確認が分⼦式および組成式の候補を絞り込むために⾮常に重要です。ChromaTOFソフトウェアでは、質量誤差、同位体存在⽐、RDBE値、窒素ルールの総合評価から独⾃のSimilarityを算出し、最も確信度の⾼い組成式を決定します。さらに決定した組成式から推定される構造式について、ChromaTOFソフトウェアからChemspiderサイトに直接移動して検索することが可能です。
下図のFig.5では、既存のCIイオン源とMMSのPCIモードについて、1 pgベンゾフェノンの クロマトグラムを⽐較しています。MMSにおけるPCI分析では、イオン化領域の表⾯温度がより均⼀であること、イオンチャンバーの密閉性が向上している等の理由から、分析感度が⼤幅に向上したことが確認できます。これは、より確実に分⼦イオンピークを検出し、⾼い精度で組成式の算出を⾏うために⾮常に有⽤です。
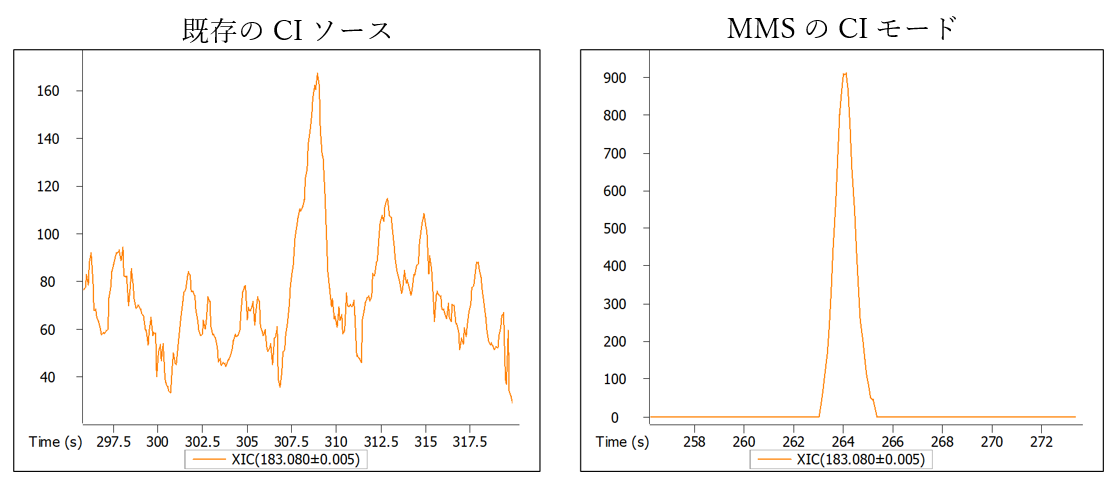
Fig.5 1 pg Benzophenoneのマスクロマトグラム⽐較
尚、ソフトイオン化法には、CI法をはじめ ⾼電界中における試料からエミッター(陽極)への電⼦移動(トンネル効果)により試料をイオン化する電界イオン化(FI:Field Ionization)法、8∼10eV程度の光エネルギーを試料分⼦に与えてイオン化する光イオン化 (PI:Photo Ionization)法などがあります。それぞれの⽅法には利点と課題となる点があり、分析機器メーカーでは、特徴を活かし課題を改善すべく理想的なイオン源の開発を⽬指しています。CI法の課題としましては、反応ガスとして可燃性ガスを使⽤することが挙げられますが、近年では試薬のヘッドスペースガスをイオン源に導⼊し、プロトン付加による化学イオン化を⾏う⽅法なども開発されています。しかしながら、CI法では、選択する反応ガスによって、試料分⼦への電荷
交換が促進されるため、試料に合わせた最適なイオン化を⾏えることが利点でもあります。また、ソフトイオン化法の中でもCI法は、感度や網羅性において優れています。
2‐3.MMSにおけるNCI測定とマススペクトル
NCI法による分析では、負イオンだけを電気的に引き出して測定し、それら負イオンは主に熱電⼦の捕獲または付着によって⽣成されます。NCIはハロゲン化合物のような電⼦親和性の⼤きな化合物を⾼感度かつ選択的に分析することができるため、その場合の感度はEI法に⽐べて数倍上がると⾔われています。またNCI分析では、電⼦捕獲を促進するため、化学的に修飾されるさまざまな種類の低分⼦に適しています。下図(Fig.6)は、DecachlorobiphenylのMMSにおけるEIおよびNCI測定結果になります。
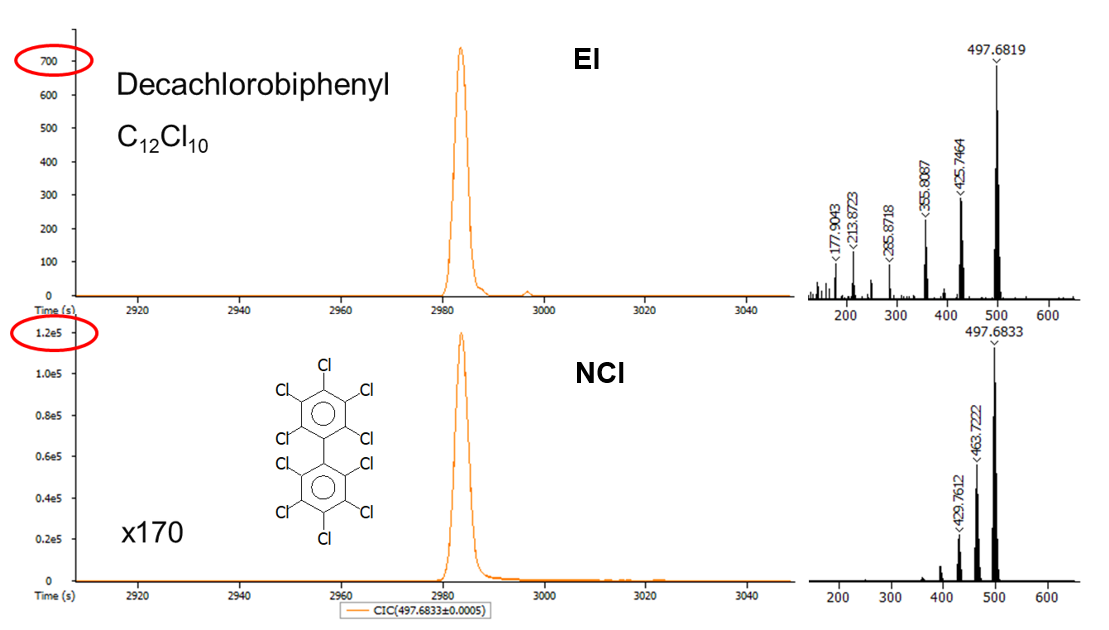
Fig.6 DecachlorobiphenylのEIとNCI測定結果
2‐4.MMSによる連続分析
MMSにおいて、イオン化モードの変更は、Mass Spectrometer Methodから⾏います。装置制御、測定から解析までをシームレスに⾏うChromaTOFソフトウェアでは、試料導⼊部(AS Method)、ガスクロマトグラフィー (GC Method)、質量分離部 (MS Method)および解析 (DP Method)など、項⽬ごとにメソッドを作成し、測定・解析を⾃動化しています。そのため、下図(Fig.7)のように、異なるイオン化法を設定したMS Methodを作成することで、同⼀の試料について各イオン化モードによる連続分析を⾏うことが可能です。
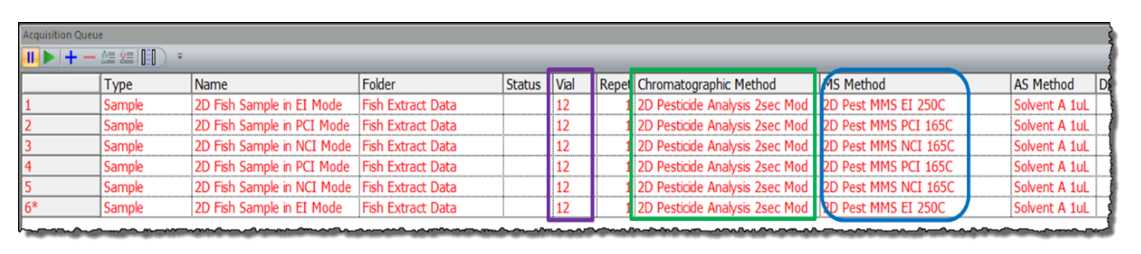
Fig.7 各イオン化モードによるシーケンステーブル
下図のFig.8および次ページのFig.9は、Fig.7のシーケンスを⽤いて連続分析を⾏ったEPA 8270 Mega Mixと有機塩素系農薬(OCP)標準の混合物試料のクロマトグラム (上からNCI、PCI、EIモード)と2-ニトロフェノールのピークの各イオン化モードによるマススペクトルになります。
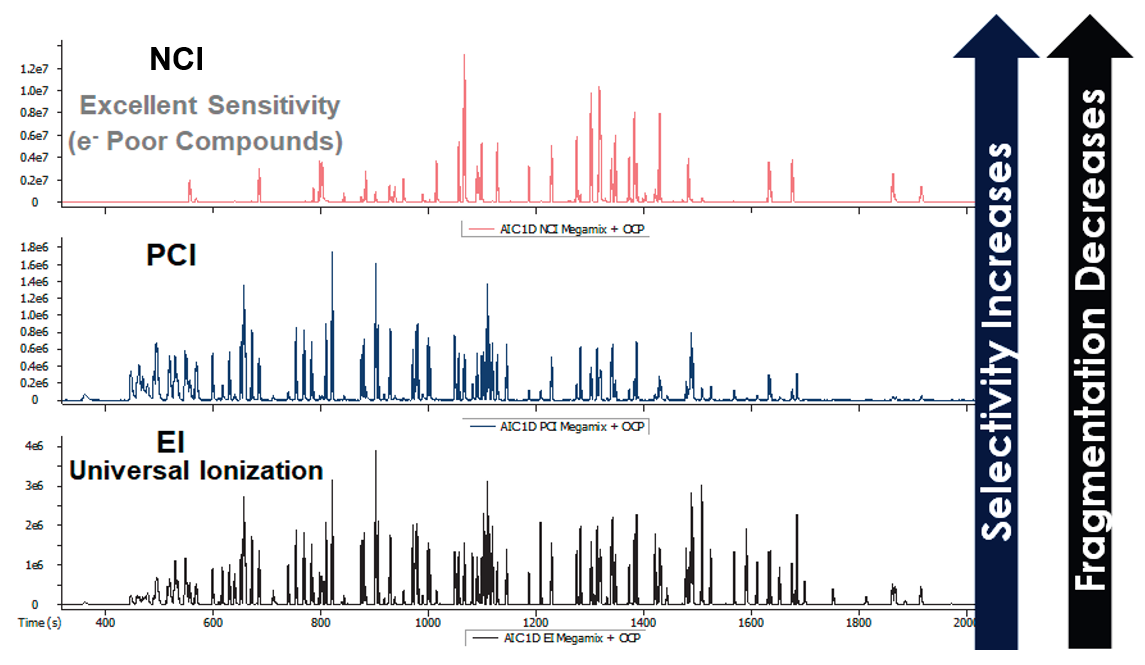
Fig.8 MMSの異なるイオン化モードによる同⼀試料のクロマトグラム各種
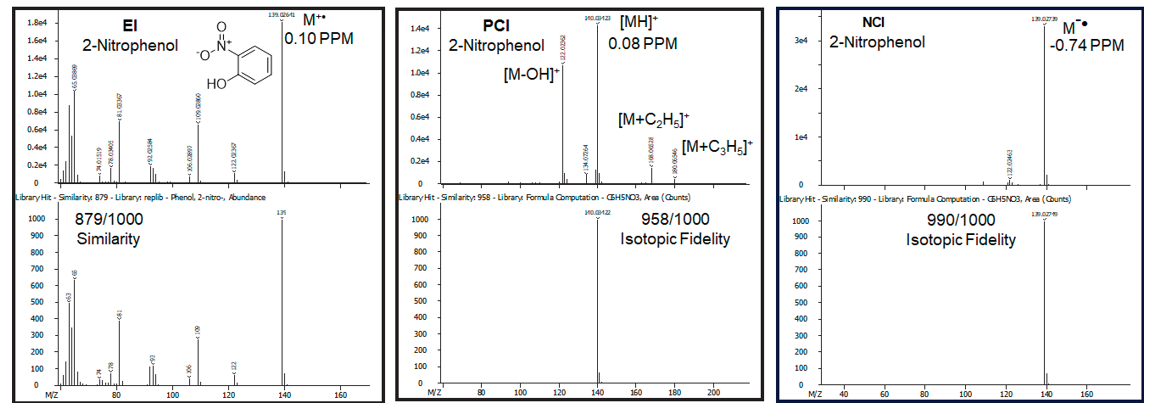
Fig.9 各イオン化モードによる2-ニトロフェノールのマススペクトル
EIスペクトルはNISTライブラリの登録スペクトルとSimilarity 879/1000で⼀致しており、分⼦イオンの質量精度は0.10ppmでした。CIスペクトルに は、プロトン付加分⼦m/z 140.03424、 m/z 168.06578[M+C2H5]+およびm/z 180.06546[M+C3H5]+の分⼦付加イオンが検出され、加えてm/z 2535=122.02362[M-OH]のフラグメントイオンが確認できました。また、分⼦イオンピークの同位体存在⽐は理論上の同位体存在⽐に対し、958/1000でした。さらにNCIスペクトルでは、フラグメントが⼤幅に減少し、m/z 139.02739に強いアニオンが確認されました。このラジカルアニオンの同位体存在⽐は理論⽐に対し990/1000と、⾮常に⾼い⼀致率を⺬しました。
3.結論
汎⽤的に利⽤するEIの感度をできるだけ損なわずに、同⼀のイオン源で CI測定を⾏うことができる新しいイオン源として「Multi-Mode Source(MMS)」を開発しました。この新しいイオン源では、EIとCIイオン源の交換作業を要することなく、これまでCI分析に消極的であったユーザーにも、気軽にPCIおよびNCI法による分析を⾏うことが可能になります。
従来のライブラリ検索には該当する化合物のない未知化合物の同定において、EIのマススペクトル解析にCI分析による分⼦量情報を組み合わせることで、解析の信頼性は⼤幅に向上します。また、各検出イオンや分⼦イオンからのニュートラルロスの組成式を算出することは、分⼦構造からのイオンの損失や開裂を予想するために重要な情報であり、これらを確実に決定することが構造を推定する上で必要不可⽋であると考えられます。
~1つのアプローチに限定しない新しいMulti-Mode Source(MMS)は、これまで同定できなかった未知化合物を解明へと導きます~

